
Expectativa por los precios
En el marco del Plan Estratégico de Vacunación contra la Covid-19, se llevará a cabo una reunión del Consejo Federal de Salud que definirá la vacunación para la franja etaria de entre 12 y 17 años con comorbilidades, con dosis del laboratorio estadounidense Moderna.
EL PAIS27/07/2021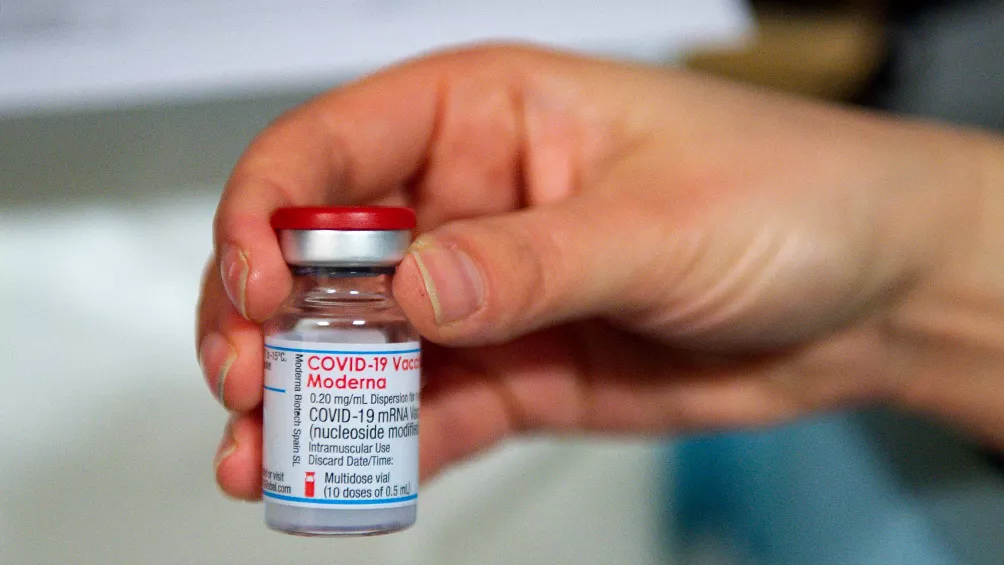
El Consejo Federal de Salud (Cofesa) se reunirá este martes para definir el inicio de la vacunación contra el coronavirus a adolescentes de entre 12 y 17 años con comorbilidades con dosis del laboratorio estadounidense Moderna, en el marco del Plan Estratégico de Vacunación contra la Covid-19.
La reunión se realizará a partir de las 9 en el Palacio San Martín de la Cancillería y participarán de manera virtual los ministros de Salud de todas las jurisdicciones del país, según informaron fuentes oficiales. Está previsto que concluya a las 18.
En el encuentro se definirá con la cartera sanitaria nacional los grupos y la estrategia de implementación y formalizarán el inicio de la vacunación para este grupo priorizado en todo el país.
En ese marco, se comenzará a vacunar a adolescentes de entre 12 y 17 años con comorbilidades, una población estimada en 900.000 personas, que para contar con el esquema completo requerirían unas 1,8 millones de dosis.
Los factores de riesgo que se evalúan incorporar son enfermedades cardíacas, neurológicas, renales, respiratorias, obesidad, algunos tipos de discapacidad y otras condiciones de vulnerabilidad.
La Agencia Europea de Medicina (EMA) aprobó el pasado viernes la vacuna del laboratorio Moderna para adolescente de 12 a 17 años, autorización que posibilita, también, el comienzo en Argentina de la vacunación para esa franja etaria.
El Gobierno nacional tiene en el centro logístico de Andreani las 3.500.000 de vacunas Moderna donadas por Estados Unidos que llegaron al país el pasado 17 de julio en dos vuelos de Aerolíneas Argentinas.
Moderna presentó los estudios de Fase III y la documentación requerida para obtener la autorización de emergencia en adolescentes tanto en la EMA como en la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA).

Expectativa por los precios

Este delito cuenta con un plan que conlleva un "ofrecimiento, una captación, transporte, traslado, acogida o recepción de personas que tiene como fin la explotación", detalló la periodista especializada Ana Inés Cabral.

El fundador de la consultora N&W Professional Traders, es considerado el intermediario entre el presidente y los creadores de la controvertida criptomoneda, habría visitado la Casa Rosada y la Residencia Presidencial de Olivos en al menos diez ocasiones.

Micaela García, de 21 años, fue una joven víctima de femicidio el 1° de abril de 2017.

Según el último informe de Indec, el 51,9% de la población de entre 0 y 14 años se ubica por debajo de la línea de la pobreza.

La piedra cae casi siempre de día, después de mucho calor y la forma de las nubes anticipada la pedrea o la granizada. Lo explica el meteorólogo Leonardo Jara , para M. POST.





Violencia urbana

Cientos de Piratas en el centro de la ciudad

Proveedores de consumidores en San Francisco

Causan daños en los campos de la región

Una historia con final abierto